
インクロムは、提携医療機関である医療法人 平心会 大阪治験病院に設置されているセントラルIRBの事務局業務を支援しております。昨今は、インクロムの提携医療機関以外の医療機関で実施する試験の審査も積極的に受託しており、幅広く事務局業務の支援に努めています。初めてセントラルIRBを使用する方、セントラルIRBの使用を迷われている方など、お気軽にお問い合わせください。
医療法人 平心会 大阪治験病院のセントラルIRBについて
医療法人 平心会 大阪治験病院の治験審査委員会(IRB)は、2005年に設置されました。
これまで幅広い疾患領域の試験の審査を数多く行っております。
また、以下の特長を有し、審議依頼者の様々な事由に応じて柔軟に対応することが可能です。
特長
◎充実した定期開催スケジュールに加え、臨時開催も提案可能
◎IRB審査を集約し、審査手続き業務と人的及び費用負担を軽減
◎経験豊富な専任スタッフによるきめ細やかなフルサポート
◎治験依頼者の説明文書雛形の事前レビュー
◎IRB機能の充実化
◎電子申請が可能
実績
IRB審査委員会開催回数(2024年12月1日現在)
2005年~ 304回
※前身である大阪臨床薬理研究所が1983年に設置したIRBは別途367回の開催実績
セントラルIRB(1試験あたり複数施設を審議)審議件数(2024年12月1日現在)
| 2施設~4施設 | 270件 |
| 5施設~9施設 | 26件 |
| 10施設~14施設 | 5件 |
| 15施設以上 | 1件 |
IRB初回審議件数(2024年12月1日現在)
健康成人対象試験
| 第Ⅰ相試験(FIH、FIJを除く) | 250件 |
| FIH(First in Human)試験 | 33件 |
| FIJ(First in Japanese)試験 | 20件 |
| 生物学的同等性試験 | 151件 |
| 生物学的利用能(bioavailability)試験 | 11件 |
| パッチ試験 | 4件 |
患者対象試験
| 内分泌代謝内科領域 | 142件 |
| 眼科領域 | 87件 |
| 循環器内科領域 | 26件 |
| 呼吸器内科領域 | 19件 |
| 耳鼻咽喉科領域 | 18件 |
| 精神神経科領域 | 11件 | 皮膚科領域 | 11件 |
| 整形外科領域 | 10件 |
| 腎臓内科領域 | 6件 |
| 泌尿器科領域 | 5件 |
| 消化器内科領域 | 3件 |
| 婦人科領域 | 2件 |
| 歯科領域 | 1件 |
セントラルIRB支援業務について
インクロムでは、セントラルIRBに関するお問い合わせ・相談窓口となり、治験依頼者のさまざまなニーズに対応いたします。実施医療機関との契約手続きやIRB費用に関する窓口も一括して対応しており、効率的かつスムーズに各種手続きを進めることが可能です。
また、IRB費用については、速やかに御見積書を提示致しますので、お気軽にお問い合わせください。
IRB費用:300,000円~(初回審査費用)
※ご予算に合わせて相談に応じておりますので、お気軽にお問い合わせください。
全ての皆様にご満足を頂けるように手厚いサポートを心掛け、効率的に審査手続きから治験契約の締結まで迅速かつ丁寧に対応いたします。
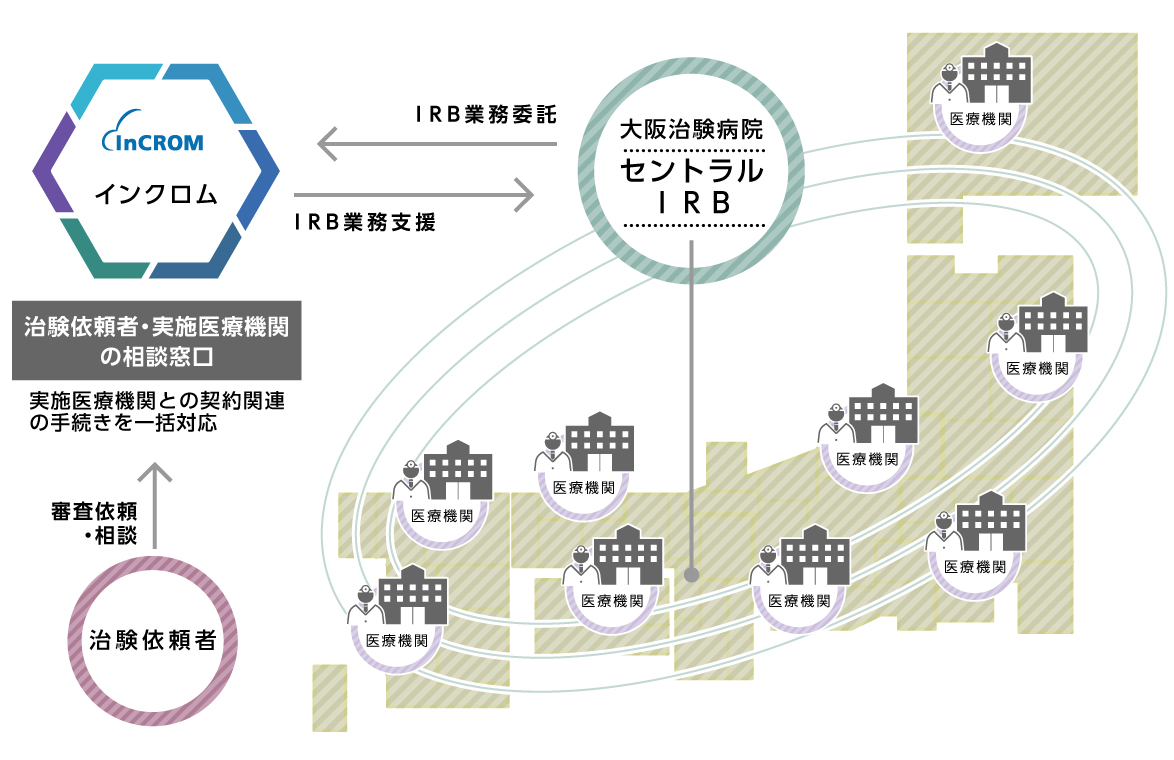
運用体制、運用フローについて
インクロムは、運用フローの図のように治験依頼者及び審査を依頼される実施医療機関を全面的に支援し、セントラルIRBの手続き等が円滑に進むように尽力いたします。
治験審査手続きの詳細について
医療法人平心会のホームページにて開催実績、開催スケジュール、審査手続きなどを詳しく解説しております。また、IRB手順書や会議の記録の概要を閲覧もしくはダウンロードして頂くことが可能です。
